Publié le
Lecture 11 mins
TheraSphereTM : une nouvelle ère grâce à la dosimétrie personnalisée
Carole ALLIMANT, service de radiologie diagnostique & interventionnelle, hôpital St-Eloi, CHU de Montpellier
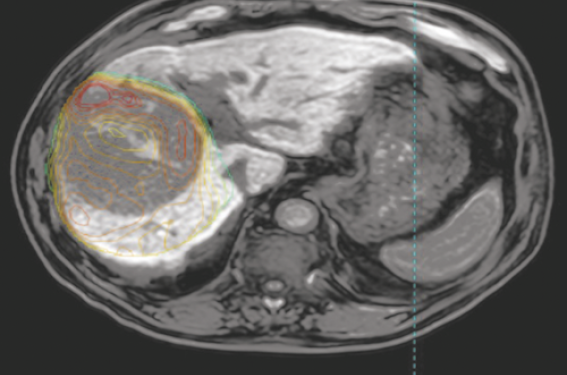
TheraSphereTM est une thérapie ciblée intrahépatique qui délivre des millions de microsphères de verre porteuses d’Ytrium 90 (Y90) radioactif.
Un produit innovant... qui fera partie de l'avenir TheraSphere TM est une thérapie ciblée intrahépatique qui délivre des millions de microsphères de verre porteuses d’Ytrium 90 (Y90) radioactif. Les premières expériences rapportées d’injection intra-artérielle datent de 1965 par Ariel et coll. sur...
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :